
На бытовом уровне мы обычно называем коррозией появление ржавчины на металле. Но, на самом деле, это лишь внешнее проявление. Наиболее неприятно то, что происходит под слоем ржавчины. А, именно, разрушение материала. Собственно, коррозия и определяется как самопроизвольное разрушение металлов и их сплавов под действием химического, электрохимического или физико-химического взаимодействия с окружающей средой. В данной статье мы будем рассматривать только электрохимическое взаимодействие, то есть, речь пойдет об электрохимической коррозии.
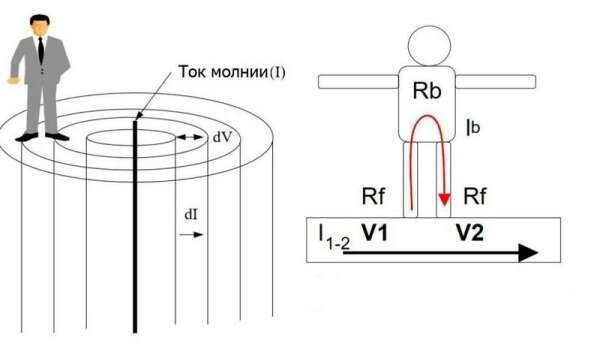
Прохождение электрического тока через электролит сопровождается перемещением ионов. Положительные ионы движутся к отрицательному электроду (катоду), отрицательные ионы – к положительному электроду (аноду). Если погрузить два электрода в электролит и пропустить через них ток, то можно наблюдать процесс постепенного растворения анода. При этом растворяемый материал частично остается в электролите, частично осаждается на катоде. Именно на этом принципе основана электрохимическая очистка металлов, а также нанесение гальванического покрытия. Но, когда все во власти стихии, перенос ионов материала приводит к печальным последствиям.
Подробнее читайте в нашей статье "Природа электрохимической коррозии".
Смотрите также:


_thumb.jpg)


